reazioni di sintesi problemi risolti (1)
inserita 04-02-2021
Problemi risolti
1- pentossido di difosforo e acqua
“ Per la teoria sulle reazioni di sintesi consultate i post: reazioni di sintesi (1) e (2) „
Scrivi la reazione di sintesi tra pentossido di difosforo e acqua per formare acido ortofosforico.
In questo esercizio i nomi dei composti, tralasciando l'acqua, sono IUPAC: pentossido di difosforo, e acido ortofosforico.
Per quanto riguarda il primo non c'è problema: il nome ci dice chiaramente come è composto: 5 atomi di Ossigeno e 2 di Fosforo.
Per quanto riguarda il secondo è invece opportuno aggiungere una postilla.
L'anidride fosforica, o pentossido di difosforo, può reagire con un numero variabile di molecole di acqua, formando 3 acidi diversi.
Equazioni di reazione: (la seconda è già bilanciata le altre 2 no)
Se reagisce con una molecola di acqua si forma l'Acido Metafosforico
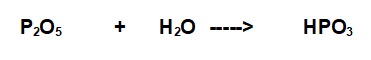
Se reagisce con due molecole di acqua si forma l'Acido Pirofosforico
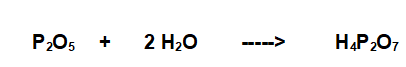
Se reagisce con tre molecola di acqua si forma l'Acido Ortofosforico (o fosforico)
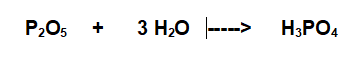
Equazioni bilanciate:
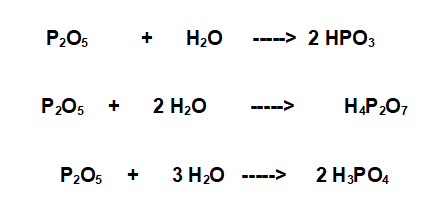
Quindi la soluzione all'esercizio è la terza!
2- anidride carbonica e acqua
“ le anidridi reagiscono con l'acqua per dare ossiacidi „
Scrivi la reazione di sintesi tra anidride nitrica e acqua per formare acido nitrico.
In questo caso il problema è che i nomi derivano dalla nomenclatura tradizionale.
L'anidride nitrica ha la desinenza in -ico, per cui l'Azoto ha il numero di ossidazione più alto.
Dato che l'azoto è al quinto gruppo il suo massimo numero di ossidazione è 5.
Considerando che l'Ossigeno è sempre -2 la formula dell'anidride Nitrica è N2O5.
L'Anidride Nitrica reagisce con una sola molecola di acqua per cui la reazione è la seguente:
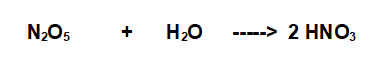
Quindi per ogni molecola di anidride e acqua che reagiscono si formano 2 molecole di Acido Nitrico, uno degli acidi più forti.
3- Completa le seguenti reazioni di Sintesi aggiungendo il reagente o il prodotto mancante e bilanciale:
“ in questi esercizi bisogna trovare uno o più reagenti o prodotti „
A- ............................. + H2 ----------> LiH
Classica formazione di un idruro metallico. L'altro reagente è quindi il Litio metallico (dato che l'idruro che si forma è l'idruro di Litio), che entra nella reazione un atomo alla volta.
Il bilanciamento è molto facile. (Vedi Le reazioni chimiche - reazioni di sintesi (2))
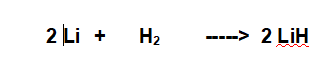
B- CO2 + H2O ------------> .............................
Classica reazione di sintesi di un ossiacido da un'anidride e acqua.
Questa è l'anidride carbonica per cui si forma l'acido carbonico. (Vedi Le reazioni chimiche - reazioni di sintesi (2))
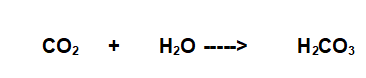
C- Al + ........................... -------------------> AlI3
Classica reazione di sintesi tra un metallo e un non-Metallo per formare un sale binario, lo Ioduro di Alluminio. Lo Iodio, ricordiamo, è una molecola biatomica. (vedi reazioni di sintesi (1) )

D- ......................... + H2O ----------------> H2SO3
Sintesi di un ossiacido, in questo caso l'acido Solforoso nel quale lo Zolfo ha un numero di ossidazione +4.
Per cui l'altro reagente sarà l'Anidride Solforosa, sempre con lo Zolfo con numero di ossidazione +4. In queste reazioni non cambia mai il numero di ossidazione del non-Metallo... (vedi reazioni di sintesi (2) )
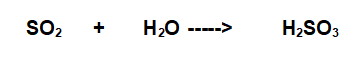
4- Completa le seguenti semireazioni di sintesi
“ In questi esercizi viene data solo la metà della reazioni, reagenti o prodotti, e bisogna scrivere l'altra metà „
A- BaO + H2O ------------> ...........................
Reazione tra un ossido basico, Ossido di Bario e Acqua. Il risultato di questo tipo di reazioni è sempre un Idrossido: in questo caso l'Idrossido di Bario. (Vedi Le reazioni chimiche - reazioni di sintesi (2))
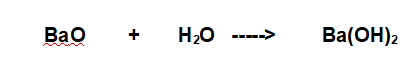
B- SO3 + H2O ---------------> .............................
Reazione analoga a quella presentata nel precedente esercizio. Reazione tra un anidride, in questo caso Anidride Solforica, lo zolfo ha numero di ossidazione +6 e acqua. Si forma un ossiacido, in questo caso l'Acido Solforico.. (Vedi Le reazioni chimiche - reazioni di sintesi (2))
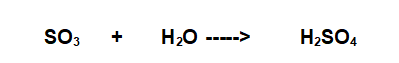
C- N2O3 + H2O ------------> ..........................
Stesso tipo di reazione della precedente, anidride + acqua per dare ossiacido. In questo caso l'anidride è l'Anidride Nitrosa, l'azoto ha numero di ossidazione +3, quindi si forma l'acido Nitroso. (Vedi Le reazioni chimiche - reazioni di sintesi (2))